
Por fin existe una tuerca giratoria NPT: cómo orientar un instrumento sin pelearte con la rosca cónica
¿Te ha pasado que… aprietas el manómetro y queda mirando a la pared? Estás montando un manómetro con rosca NPT.Vas apretando, parece que ya sella…
Temita controvertido en nuestro sector, es realmente uno de estos que no quieres que te venga un problemón encima la mesa cuando te llaman por una no conformidad de corrosión.
A continuación, te explicaré de manera resumida el catastrófico impacto que puede llegar a tener la corrosión galvánica con un ejemplo basado en hechos verídicos:
En 1763, la fragata inglesa llamada “Alarm” sufrió las consecuencias de la corrosión galvánica. El caso es que decidieron realizar un revestimiento de cobre sobre la nave para proteger el casco de madera contra gusanos marinos y percebe. El problema radica en que adhirieron el revestimiento de cobre usando clavos de hierro. Por la diferencia de potencial de estos dos elementos, y la aparición del electrólito (agua salada), se formó una corrosión galvánica que puso en peligro la funcionalidad de la nave, la integridad estructural y por ende la seguridad de la tripulación a bordo.
En este post vamos a comentar la corrosión galvánica, un fenómeno electroquímico, el cual si no se tiene en cuenta puede llegar a causar grandes consecuencias en la durabilidad y rendimiento de los materiales metálicos. Se lo puede cargar todo y simplemente por la mala selección de los metales en contacto entre ellos.

Se deberán de cumplir las siguientes condiciones:
Por tanto, como se ha podido observar a lo largo de esta explicación, la corrosión galvánica tiene una gran relevancia en las industrias que estén en contacto con electrólitos como el agua de mar, como puede ser industrias de construcción naval, desalinizadoras, EDAR y cualquier planta que se encuentre cerca de ambientes donde se encuentre agua salada.
Pero vamos a la parte interesante…
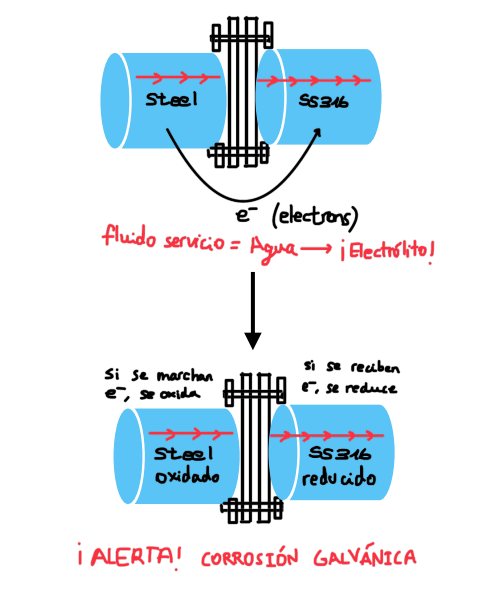
A continuación, dejamos a vuestro servicio un sistema que permite saber de manera precisa si la unión de esos materiales acabará resultando en corrosión galvánica, o si, por el contrario, te puedes olvidar de este problema.
En Redfluid, disponemos de una gran variedad de materiales en prácticamente todo lo que estés buscando relacionado con fittings y válvulas, ya sea de baja o alta presión (sector en el que somos especialistas).
Espero que haya quedado todo bastante más claro, y ya sabéis, cualquier consulta que tengáis os podéis poner en contacto con nosotros para que os la podamos aclarar 🙂
Comparte este artículo

¿Te ha pasado que… aprietas el manómetro y queda mirando a la pared? Estás montando un manómetro con rosca NPT.Vas apretando, parece que ya sella…

Imagina que en una instalación de tuberías necesitas desmontar una sección para dar mantenimiento o reemplazar un componente. Tener que desroscar tramos enteros de tubería,